مقدمه
زردی نوزادان (Jaundice) یکی از شایعترین مشکلاتی است که والدین پس از تولد فرزند خود با آن روبهرو میشوند. این عارضه با تغییر رنگ پوست و چشم نوزاد به زردی مشخص میشود. در بسیاری از موارد، زردی خوشخیم است، اما گاهی میتواند نشانه یک مشکل جدیتر باشد و نیاز به پیگیری و آزمایش تشخیص زردی نوزادان دقیق داشته باشد.
درک درست از ماهیت زردی، علل بروز آن، زمان مراجعه به پزشک و روشهای درمانی، برای والدین و ارائهدهندگان مراقبتهای بهداشتی اهمیت ویژهای دارد. هدف این مقاله، ارائه اطلاعات جامع و کاربردی درباره زردی نوزادان با تمرکز بر تشخیص آزمایش تشخیص زردی نوزادان، روشهای درمانی و مراقبتهای ضروری است تا والدین بتوانند با آگاهی کامل بهترین تصمیم را برای حفظ سلامت نوزاد خود بگیرند.
زردی چیست و چرا اتفاق میافتد؟
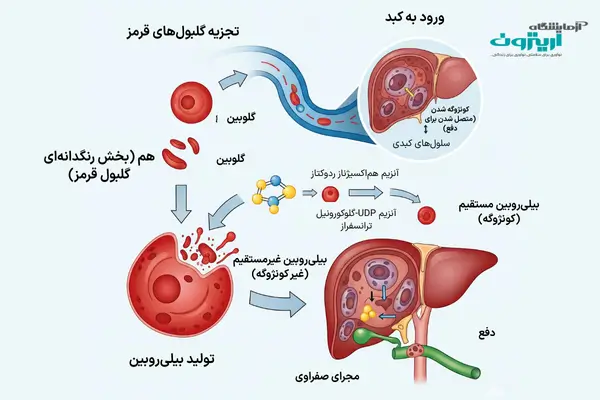
زردی نوزادان ناشی از افزایش سطح بیلیروبین (Bilirubin) در خون است. بیلیروبین یک رنگدانه زردرنگ محسوب میشود که در نتیجه تجزیه گلبولهای قرمز خون بهوجود میآید. در حالت طبیعی، کبد این رنگدانه را از خون جمعآوری کرده و آن را به شکلی قابل دفع (از طریق مدفوع) تبدیل میکند. اما در نوزادان، به دلایل مختلف ممکن است این فرآیند بهطور کامل انجام نشود و در نتیجه بیلیروبین در خون تجمع پیدا کند. همین موضوع یکی از دلایل اصلی مراجعه به پزشک و انجام آزمایش تشخیص زردی نوزادان است.
انواع زردی در نوزادان
1. زردی فیزیولوژیک (Physiological Jaundice):
این شایعترین نوع زردی است که تقریباً در ۶۰ درصد نوزادان ترم و ۸۰ درصد نوزادان نارس دیده میشود. کبد نوزاد در روزهای ابتدایی زندگی هنوز بهطور کامل بالغ نشده و قادر به پردازش سریع بیلیروبین نیست. این نوع زردی معمولاً در روز دوم یا سوم پس از تولد ظاهر شده، در روز چهارم یا پنجم به اوج میرسد و طی یک تا دو هفته بهتدریج برطرف میشود. هرچند این حالت اغلب بیخطر است، اما نیاز به پایش و در صورت لزوم انجام آزمایش تشخیص زردی نوزادان دارد.
2. زردی پاتولوژیک (Pathological Jaundice):
این نوع زردی کمتر شایع است، اما میتواند نشاندهنده یک بیماری یا اختلال جدیتر باشد. مهمترین علل زردی پاتولوژیک عبارتاند از:
- ناسازگاری گروه خونی (ABO یا Rh): بدن مادر آنتیبادیهایی تولید میکند که به گلبولهای قرمز نوزاد حمله کرده و موجب تخریب آنها میشود؛ در نتیجه سطح بیلیروبین افزایش مییابد.
- کمبود آنزیم G6PD: یک اختلال ژنتیکی که باعث تخریب زودهنگام گلبولهای قرمز میشود.
- عفونتها (Sepsis): عفونتهای شدید در نوزاد میتوانند سطح بیلیروبین را بالا ببرند.
- بیماریهای کبدی: اختلالات مادرزادی یا عفونتهای کبدی ممکن است مانع دفع صحیح بیلیروبین شوند.
- انسداد مجاری صفراوی (Biliary Atresia): یک بیماری نادر که در آن مجاری صفراوی آسیب دیده یا مسدود هستند.
- سفالوهماتوم (Cephalohematoma): تجمع خون زیر پوست سر نوزاد به دلیل آسیب هنگام زایمان که در اثر تجزیه میتواند منجر به افزایش بیلیروبین شود.
- زردی ناشی از شیر مادر (Breast milk jaundice): در موارد نادر، ترکیبات موجود در شیر مادر فرآیند دفع بیلیروبین توسط کبد نوزاد را کند میکنند. این نوع معمولاً بیخطر است و به مرور برطرف میشود.
- زردی ناشی از تغذیه ناکافی (Breastfeeding jaundice): در هفته اول زندگی ممکن است به دلیل دریافت ناکافی شیر توسط نوزاد، دفع بیلیروبین کاهش پیدا کرده و زردی ایجاد شود.
علائم زردی نوزادان
بارزترین نشانه زردی، تغییر رنگ پوست و صلبیه (بخش سفید) چشم نوزاد به رنگ زرد است. معمولاً این تغییر ابتدا در سر و صورت ظاهر میشود و بهتدریج به سمت قفسه سینه، شکم و سپس پاها پیشروی میکند. برای بررسی اولیه زردی، میتوانید پوست نوزاد را بهآرامی در ناحیه پیشانی یا بینی فشار دهید؛ اگر پس از برداشتن فشار، رنگ پوست متمایل به زرد بود، احتمال بروز زردی وجود دارد. در چنین شرایطی، بهترین اقدام مراجعه به پزشک و انجام آزمایش تشخیص زردی نوزادان است تا سطح بیلیروبین بهطور دقیق مشخص شود.
چه زمانی باید نگران زردی بود و به پزشک مراجعه کرد؟
اگرچه بیشتر موارد زردی فیزیولوژیک و بیخطر هستند، اما در صورت مشاهده هر یک از علائم زیر، مراجعه فوری به پزشک ضروری است:
- بروز زردی در ۲۴ ساعت اول پس از تولد (علامتی هشداردهنده که همیشه نیازمند بررسی است).
- افزایش سریع شدت زردی.
- انتشار زردی به دستها و پاها (نشاندهنده سطوح بالای بیلیروبین).
- خوابآلودگی بیش از حد و بیحالی نوزاد؛ بهطوری که به سختی بیدار میشود یا خوب شیر نمیخورد.
- تغذیه نامناسب یا مکیدن ضعیف.
- گریه با صدایی بلند و غیرعادی.
- تب.
- مدفوع رنگپریده (سفید یا خاکستری) یا ادرار تیره، که میتواند نشانه اختلالات کبدی باشد.
- ادامهدار بودن زردی بیش از دو هفته در نوزادان ترم یا سه هفته در نوزادان نارس.
آزمایش تشخیص زردی نوزادان
انجام بهموقع و دقیق آزمایش تشخیص زردی نوزادان نقش حیاتی در پیشگیری از عوارض جدی دارد. روشهای اصلی تشخیص عبارتاند از:
1.معاینه فیزیکی:
پزشک نوزاد را از نظر تغییر رنگ پوست و چشمها بررسی کرده و میزان شدت و پیشرفت زردی را ارزیابی میکند.
2. بیلیروبین پوستی (Transcutaneous Bilirubinometer – TcB):
این روش غیرتهاجمی با استفاده از دستگاهی روی پوست نوزاد انجام میشود و میزان تقریبی بیلیروبین را نشان میدهد. TcB برای غربالگری اولیه بسیار کاربردی است، اما اگر سطح آن بالا باشد، نیاز به آزمایش خون جهت تأیید وجود دارد.
3. آزمایش خون بیلیروبین سرم (Serum Bilirubin Test):
دقیقترین و مهمترین روش برای تشخیص آزمایش تشخیص زردی نوزادان، آزمایش خون است. در این روش با گرفتن نمونه کوچکی از خون نوزاد (معمولاً از پاشنه پا)، سطح بیلیروبین کل (Total Bilirubin)، بیلیروبین مستقیم (Direct Bilirubin) و بیلیروبین غیرمستقیم (Indirect Bilirubin) اندازهگیری میشود:
- بیلیروبین غیرمستقیم (غیر کونژوگه): شکلی از بیلیروبین که هنوز توسط کبد پردازش نشده و عامل اصلی زردی در بیشتر نوزادان است. سطوح بالای آن میتواند خطرناک باشد.
- بیلیروبین مستقیم (کونژوگه): بیلیروبینی که توسط کبد پردازش شده و آماده دفع است. افزایش این نوع همیشه پاتولوژیک محسوب میشود و نیاز به بررسی دقیقتر برای یافتن علت زمینهای (مانند مشکلات کبدی یا انسداد صفراوی) دارد.
4. سایر آزمایشها در موارد مشکوک به زردی پاتولوژیک:
- تعیین گروه خونی مادر و نوزاد به همراه تست کومبس (Coombs Test) برای بررسی ناسازگاریهای خونی.
- شمارش کامل خون (CBC) جهت ارزیابی کمخونی یا عفونت.
- سنجش سطح آنزیم G6PD در صورت مشکوک بودن به کمبود آن.
- آزمایشهای عملکرد کبد برای بررسی سلامت کبد.
- کشت خون یا ادرار برای تشخیص عفونت احتمالی.
اهمیت آزمایشگاه اریترون در تشخیص زردی نوزادان
آزمایشگاه اریترون با بهرهگیری از تجهیزات پیشرفته و تیمی متخصص، آماده ارائه دقیقترین خدمات در زمینه آزمایش تشخیص زردی نوزادان است. دقت در اندازهگیری سطح بیلیروبین و سایر پارامترهای مرتبط، کلید اصلی اتخاذ تصمیمات درمانی صحیح و بهموقع به شمار میرود. ما متعهد هستیم با ارائه نتایج سریع و قابل اعتماد، به پزشکان و والدین در مدیریت بهینه زردی نوزادان کمک کنیم.
درمان زردی نوزادان
هدف اصلی درمان، کاهش سطح بیلیروبین در خون برای جلوگیری از بروز عوارض جدی مانند کرنیکتروس (Kernicterus) است. کرنیکتروس نوعی آسیب مغزی برگشتناپذیر است که در اثر رسوب بیلیروبین بالا در بافتهای مغزی ایجاد میشود. روشهای درمانی بر اساس شدت زردی، سن نوزاد و علت زمینهای انتخاب میشوند:
1. تغذیه مکرر با شیر مادر یا شیر خشک:
افزایش دفعات شیردهی (حدود 8 تا 12 بار در 24 ساعت) به نوزاد کمک میکند بیلیروبین اضافی از طریق مدفوع دفع شود. همچنین، تغذیه کافی از کمآبی بدن جلوگیری میکند که خود میتواند عامل تشدید زردی باشد.
2. نوردرمانی (Phototherapy):
این روش شایعترین و مؤثرترین درمان برای زردی شدید است. نوزاد در زیر نورهای آبی مخصوص (یا پتوی نوری) قرار داده میشود. نور باعث تغییر ساختار بیلیروبین غیرمستقیم شده و آن را به شکلی قابل دفع از طریق ادرار و مدفوع تبدیل میکند. در طول نوردرمانی، چشمهای نوزاد با پوشش محافظ پوشانده میشوند.
3. تعویض خون (Exchange Transfusion):
در موارد بسیار شدید که نوردرمانی مؤثر نیست یا خطر کرنیکتروس بالاست، تعویض خون انجام میشود. در این روش، بخشی از خون نوزاد با خون اهدایی جایگزین میشود تا بیلیروبین و آنتیبادیهای مضر (در صورت ناسازگاری خونی) از بدن خارج شوند.
4. دارودرمانی (Pharmacological Treatment):
در برخی شرایط خاص، داروهایی مانند فنوباربیتال (Phenobarbital) ممکن است برای تقویت توانایی کبد در پردازش بیلیروبین تجویز شوند، هرچند این روش کمتر رایج است.
- ایمونوگلوبولین وریدی (IVIG): در موارد شدید ناسازگاری خونی، IVIG میتواند برای کاهش تخریب گلبولهای قرمز توسط آنتیبادیهای مادر استفاده شود.
5. درمان علت زمینهای:
اگر زردی ناشی از بیماریهایی مانند عفونت یا اختلالات کبدی باشد، درمان آن بیماری برای رفع زردی ضروری است.
مراقبتهای پس از ترخیص و پیگیری
حتی پس از ترخیص نوزاد از بیمارستان، نظارت بر وضعیت زردی اهمیت زیادی دارد. والدین باید بهطور منظم علائم را بررسی کرده و در صورت مشاهده هرگونه تغییر یا تشدید، فوراً با پزشک تماس بگیرند. همچنین، ویزیتهای منظم پس از تولد، بهویژه برای نوزادانی که در معرض خطر بالاتر هستند، بسیار ضروری است.
پیشگیری از زردی شدید
اگرچه امکان پیشگیری کامل از تمام موارد زردی وجود ندارد، اما برخی اقدامات میتوانند خطر بروز زردی شدید را کاهش دهند:
- تغذیه مکرر و کافی نوزاد: اطمینان از اینکه نوزاد به میزان کافی شیر دریافت میکند.
- تشخیص زودهنگام و درمان بهموقع: انجام غربالگریهای لازم و مراجعه به پزشک در صورت بروز علائم اولیه زردی.
- شناسایی عوامل خطر: پزشک باید عواملی مانند گروه خونی مادر و نوزاد، سابقه زردی در خواهر یا برادر، یا تولد نارس را مدنظر قرار دهد.
کرنیکتروس (Kernicterus) و عوارض جدی زردی
کرنیکتروس جدیترین عارضه زردی شدید است. زمانی که سطح بیلیروبین غیرمستقیم (که محلول در چربی است) بیش از حد بالا رود و از سد خونی-مغزی عبور کند، در بافت مغز رسوب کرده و به سلولهای مغزی آسیب دائمی وارد میکند.
علائم کرنیکتروس شامل بیحالی شدید، مکیدن ضعیف، سفتی بدن، تب و گریههای بلند و غیرعادی است. در مراحل پیشرفتهتر، ممکن است تشنج یا کما نیز رخ دهد. عوارض طولانیمدت این وضعیت شامل فلج مغزی، کاهش شنوایی، مشکلات بینایی و اختلالات تکاملی و ذهنی خواهد بود.
به همین دلیل، انجام آزمایش تشخیص زردی نوزادان بهموقع و مدیریت صحیح آن اهمیت فوقالعادهای دارد و میتواند از بروز این عوارض پیشگیری کند.
نتیجهگیری
زردی نوزادان یک وضعیت شایع است که در اکثر موارد خوشخیم بوده و به خودی خود یا با مداخلات ساده درمانی برطرف میشود. با این حال، اهمیت آزمایش تشخیص زردی نوزادان به موقع و پیگیری دقیق را نمیتوان نادیده گرفت.
والدین باید نسبت به علائم زردی هوشیار باشند و در صورت مشاهده هرگونه نگرانی، فوراً با پزشک مشورت کنند. آزمایشگاه اریترون با ارائه خدمات آزمایش تشخیص زردی نوزادان دقیق و قابل اعتماد، در کنار شماست تا با اطمینان خاطر، سلامت فرزند دلبندتان را تضمین کنید. آگاهی و اقدام به موقع، کلید اصلی در حفظ سلامت و آینده نوزادان ماست.
سوالات متداول
- زردی نوزاد از چه زمانی خطرناک است؟
اگر زردی در 24 ساعت اول پس از تولد ظاهر شود یا شدت آن سریعاً افزایش یابد، نیاز به بررسی فوری دارد. - چگونه میتوان زردی نوزاد را تشخیص داد؟
تغییر رنگ پوست و چشمها اولین علامت است، اما روش قطعی، انجام آزمایش تشخیص زردی نوزادان توسط پزشک است. - آیا همه نوزادان به درمان زردی نیاز دارند؟
خیر. بسیاری از موارد زردی فیزیولوژیک بدون درمان خاص برطرف میشوند، اما برخی نیاز به نوردرمانی یا اقدامات دیگر دارند.